
(1)若向A中滴加稀盐酸,有气泡产生,则A中一定有 。
(2)若向B中滴加稀盐酸,无现象,则B中一定含有的金属离子是 ,可能含有的金属离子是 。
18.A、B、C、D、E是初中化学中常见的化合物,其中A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,它们的关系如图1-5所示。

图1-5
请回答下列问题。
(1)白色沉淀E为 。
(2)若现象I为“生成白色沉淀”,则A的化学式可能为 (写出一种即可);反应②的化学方程式为 。
(3)若现象I为“无明显变化”,则A的化学式可能为 、 等。
三、实验题(共2个小题,每空1分,每个化学方程式2分,共14分)
19.图1-6装置常用于实验室制取气体。根据给出的装置回答下列问题。

图1-6
(1)实验室利用氯酸钾和二氧化锰制取氧气,应选择的发生装置是 。利用C装置收集氧气的最佳时刻是 。用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是 (用化学方程式表示)。
(2)使用B装置制取气体的突出优点是 。若改用F装置收集二氧化碳,则气体应从 端进入。制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→
(用端口字母表示)。
20.化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭。”他们决定探究CO2与Na反应的产物。
[提出猜想] CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3。
[查阅资料] ①Na是非常活泼的金属,常温下与O2、H2O等物质反应。
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应。
③Na2O是白色固体,与H2O反应生成NaOH。
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀。
[实验过程] 同学们在老师的指导下设计了如图1-7所示装置(部分夹持仪器已略去)。
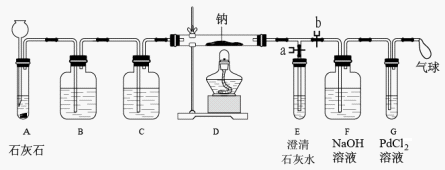
图1-7
(1)实验记录
|
序号 |
实验操作 |
主要实验现象 |
实验结论和解释 |
|
① |
打开a,关闭b, 由长颈漏斗注入稀盐酸 |
A中产生大量气泡; E中出现浑浊 |
E中反应的化学方程式为_____________ |
|
② |
当E中出现浑浊时,打开b,关闭a,点燃酒精灯 |
D中Na剧烈燃烧,产生白烟,内壁附着黑色、白色固体; G中产生黑色沉淀 |
反应产物一定有_______和_______ |
|
③ |
取D中白色固体于试管中, 加水溶解,再加入石灰水 |
产生白色沉淀 |
反应产物还有________ |
(2)实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是___________________________。
②若无装置C,对实验有影响的物质是__________。
③检验第4种物质是否存在的实验方案:取D中白色固体于试管中
。
四、计算题(共9分)
21.将一包氯化钠和碳酸钠的固体混合物溶于 50.1 g 水制成溶液,然后向其中加入溶质的质量分数为10%的氯化钙溶液至反应刚好完全时,生成沉淀 10 g,将滤液蒸干后得到固体25 g。求:
(1)原固体混合物中氯化钠的质量。
(2)共用去氯化钙溶液多少克?
(3)反应后所得滤液中溶质的质量分数?
 ,我们将会及时处理。
,我们将会及时处理。