
|
实验编号 |
实验操作 |
实验现象 |
|
① |
将气体通入澄清石灰水中 |
澄清石灰水#FormatImgID_52#变浑浊 |
|
② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】
(1)由实验①可知,该气体中肯定含有
,写出该反应的化学方程式:
。
(2)由实验②不能确定该气体中不含氧气,理由是 。
【拓展延伸】向维C泡沸片溶液中滚圆石蕊试液,溶液变红,说明溶液显 性。
27、(8分)氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,请写出该反应的化学方程式 。
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液。经检验滤渣的成份是碳酸钙。
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因 。
【实验证明】
|
实验 |
现象 |
结论 |
|
实验一:取滤液,向其中滴入少量碳酸钠溶液 |
Ⅰ: |
猜想二不成立 |
|
实验二:另取滤液,向其中加入足量 |
Ⅱ:产生气泡 |
猜想 成立 |
【反思与拓展】
(1)向CaH2和足量水反应后的溶液加入NH4Cl溶液,产生的气体是 。
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是 。
四、计算题 (共11分)
28、(4分)丁二酮(C4H6Ox)可用作糖果增香剂。请计算:
(1)丁二酮是由 元素组成的。
(2)碳元素和氢元素的质量比为 。
(3)丁二酮的相对分子质量为86,则x 的数值为 。
(4)
17.2g的丁二酮含碳元素的质量为 g。
29、(7分)硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅。向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示。
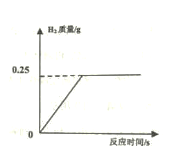
试回答:(计算结果精确到0.1% )
(1)硅钢合金属于 材料(选填“金属”或“有机物”)
(2)硅钢合金中铁的质量分数。
(3)反应结束后所得溶液溶质质量分数。
 ,我们将会及时处理。
,我们将会及时处理。