
四、实验与探究题(本大颐包括3 小颐,共25 分)
21.(7分)下面是“燃烧的条件”实验活动的部分操作示意图:
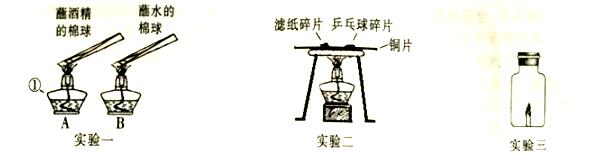
(l)仪器①的名称为___________;
(2)实验一加热片刻观察到A中棉球上的酒精燃烧产生蓝色火焰,B中棉球上的水不燃烧,由此得出燃烧的条件之一是__________;
(3)实验二观察到先燃烧的物质是__________;若将铜片上的物质换成等量的木屑和煤粉进行实验,观察到木屑先燃烧,说明木屑的着火点比煤粉__________;

(4)实验三将燃着的蜡烛放在如图所示的密闭容器中,同时用氧气传感器侧出密闭容器中氧气含量的
变化如右图所示,下列说法错误的是_______(填序号)。
A.蜡烛燃烧需要氧气
B.蜡烛燃烧前,密闭容器中氧气的体积分数为21%
C.蜡烛熄灭后,密闭容器中还有氧气
D.蜡烛熄灭后,密闭容器中的二氧化碳体积分数为84%
22.(9分)为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1. H2和CO2;猜想2. CO和H2O。
【设计实验】20℃时,甲酸的状态为______;从图一装置中选择合适的装置______(填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。
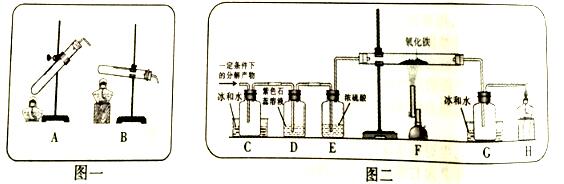
【实验预测】若猜想l成立,则D中的实验现象应为______。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为______,甲酸分解的化学方程式为______。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3. H2O和CO2;猜想4.CO和H2O。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是______。
23.(9分)兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末.将少量柠檬酸和这种白色粉未溶于水,混合后产产生了使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:
【提出猜想】猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠
【查阅资料】①碳酸钠溶液、碳酸氢钠
溶液均呈碱性;
② 碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解
【实验探究】 小月、小妮分别对有关猜想设计方案并进行实验:
|
|
实验操作 |
实验现象 |
实验结论 |
|
小月 |
将白色粉末溶于水后用pH试纸测定其酸碱度 |
pH_____7(填“>”、“<”或“=”) |
溶液呈碱性,猜想1成立 |
|
小妮 |
用下图所示的装置进行实验 |
试管A中有水珠产生,试管B中液体变浑浊 |
猜想2成立,试管B中反应的化学方程式为___________。 |

【交流反思】大家一致认为小月和小妮的结论不准确:
(1)小月实验结论不准确的原因是_____________;
(2)小妮的实验方案不能排除白色粉末是否含有_______。
【继续探究】小戚称取mg白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为n g,通过计算并分析实验数据确定猜想3正确,则n的取谊范围为_______(用含m 的代数式表示)。
【结论分析】探究后他们核查到添加剂的成分是柠檬酸和碳酸氧钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
【拓展应用】下列物质常温下放置一段时间也会分解的是_______(填序号)。
A.浓硫酸 B.氢氧化钠 C.碳酸氢铵 D.氯化钠
五、计算题(本大题包括1小题,共10分)
24. ( 10 分)学习小组测定某工业废水(含有H2SO4、HNO3,不含固体杂质)中H2SO4的含量。取100g废水于烧杯中,加入100gBaCl2溶液,恰好完全反应,经过滤得到176.7g溶液。
(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为_______g;
(2)该工业度水中硫酸的质量分数为多少?(写出计算过程)[来源:学科网]
(3)为避免工业废水污染环境,排放前应对废水进行中和处理,需加入的物质是________。
 ,我们将会及时处理。
,我们将会及时处理。