����1.���л������ڸ��Ϸ��ϵ���
����A.NH4HCO3 B.K2SO4 C.KNO3 D.Ca(H2PO4)2
����2. )������������pH=2��ˮ��Һ�д����������
����A.SO42-��NO3-��K+��OH- B.HCO3-��Cl-��SO42-��Na+
����C.Cl-��NO3-��K+��Na+ D.NH4+��Cl-��OH-��K+
����3. ũ����������Ҫ���϶൪���ס���Ԫ�صĻ��ʣ����л������ں����Ϸ��ϵ���C
����A.NH4NO3 B.Ca(H2PO4)2 C.(NH4)2HPO4 D.KNO3
����4.���и��������ܹ�����Һ�д����������A
����A. KCl��NaNO3 B. HCl��NaHCO3
����C.NaCl��AgNO3 D.H2SO4��NaOH
����5. ijũ��վ�����ϴ��۵Ļ�����NH4 N03 ��KNO3 ��CO( NH2 )2������ȱ�ٵķ���Ʒ����(B )
����A .���� B .�� C .�ط� D .���Ϸ�
����6. ������������ӵ��γ�Ϊ�����Σ������������������ε���(C )
����A��H2SO4 B ��Na2S C��K2SO4 D ��S02
����7. ���ڵ��ʵ���( C )
����A��K2CO3 B��Na2CO3 C��NH4HCO3 D��Ca(H2PO4)2
����8.�ڻ��������[Ca2(PO4)2]����( C )
����A.�ط� B.���� C.�� D.���Ϸ�
����9.�������ڸ��Ϸ��ϵ���(C )
����A. NaNO3 B.K2SO4 C.NH4H2PO4 D.Ca3(PO4)2
����10. ���и���������ˮ���ܴ����������( B )
����A.Na+��H+��Cl-��HCO3- B.Na+��K+��NO3-��Cl-
����C.H+��Na+��OH-��SO42- D.Ag+��Ca2+��Cl-��NO3-
����11.��ʢ��5g16%��NaOH��Һ�Ķ��Թܷ���ʢ��l0g16%��CuS04��Һ����ƿ���ͼ��ʾ����б��ƿֱ��ʹ����Һ��ֻ�ϣ���Ϻ��ܵ���( D )
����A.������ɫ����0.98g
����B.��ƿ����������������
����C.������Һ��Na2S04������������9.5%
����D.���õ�Na2S04��Һ������ԭCuS04��Һ�������
����12. �����������ڵ��ʵ���D
����A.��ʯ�� B.����� C.������� D.�Ȼ��
����13.�ֱ����и�������ͬʱ���뵽����ˮ�У������ܵõ���ɫ������Һ����(C )
����A.NaOH H2SO4 BaCl2 B.NaOH CuSO4 NaCl
����C.HNO3 KNO3 K2SO4 D.Na2SO4 FeCl3 KCl
����14.��ѧ���϶���ʳ����������Ҫ���ã����������ʵ���D
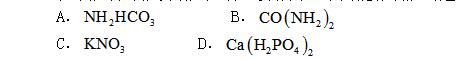
����15.����������θ�����֢��������C
����A.����B.ʳ��C.С�մ� D.ʳ��
����16.�����йػ��ʺ�ũҩ��˵���������C
����A���Ȼ��ؿ������ط�
����B����������Ч���ũ�������
����C��ũҩʩ�ú���ͨ��ũ����ת�Ƶ�����
����D��ũҩӦ����ũ����溦��ũҩ���ص����ʩ��
����17.���±�����ʵ�飬�й�˵���������������D

����A��������ɫ����
����B���ڷ�Ӧ�Ļ�ѧ����ʽΪ��CuSO4+BaCl2=BaSO4��+CuCl2
����C��������Ӧ�����ڸ��ֽⷴӦ
����D��ֻҪ�г������ɵķ�Ӧ�����ڸ��ֽⷴӦ
����18.ũҵ������Ҫ����ʹ�ø�����ϡ����л��������ʵ���D
����A.NH4Cl B.K2SO4 �� C.KNO3�� D.Ca(H2PO4)2
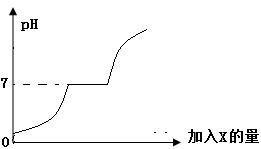
����19.���������CaCl2�Ļ����Һ����������μ��� ������ij����X����Һ��pH�����X�����ı仯��ϵ������ͼ��ʾ����X������B
����A��ˮ
����B��������Һ
����C������ʯ��ʯ
����D��ϡ����
����20.����[CO(NH2)2]��һ�ֳ����Ļ�ѧ���ϣ������ڣ�C
����A. �ط� B. �� C. ���� D. ũ�ҷ�
����21.������������������ˮ�и������������������е�����(��������һ����ͬ������)��H+��Cu2+��K+��NO3-��OH-�������������ŷŶ���������ص���Ⱦ;������������ˮ��һ��������ϣ���������ˮ����ֻ����һ�����ʵ���ɫ������Һ������Һ�������ʡ����й�����ˮ�ķ�������ȷ���� (C )
����A.OH�C��Cu2+����ͬһ���� B.Cu2+��K+����ͬһ����
����C.K+��OH�C����ͬһ���� D.H+��K+����ͬһ����
����21.���з������ڸ��Ϸ��ϵ���B
����A.NH4NO3 B.KNO3 C.KCl D.Ca(H2PO4)2
����22.���и��������� pH =1 ����Һ���ܴ����������A
����23.�������������ڸ��Ϸ��ϵ���(A��)
����A. KNO3 B. NaNO3 C. Na3PO4 D. KCl
����1�����ȽϹ��ɷ�����ѧϰ��ѧ��һ����Ҫ������(���D����ʾ���������������ܷ�����Ӧ����������ʾij�����ʿ�ͨ��һ����Ӧת��Ϊ��һ�����ʡ�)
����(1) ���Ա�2����Ţ�Ϊʾ������д��� �� �еĿո�
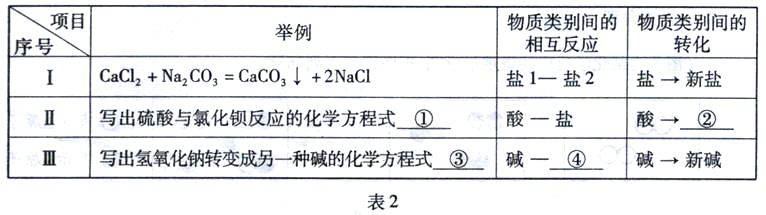
����(2) �����£��Ȼ�þ���������ʵı仯��ϵ����ȷ����____________(����)��
����A. MgCl2 �� AgNO3 B. KNO3 �� MgCl2
����C. MgCl2 �� HCl D. Mg(OH)2 �� MgCl2
������ �� H2SO4 + BaCl2 = 2HCl + BaSO4�� �� ����(��������)
������ CuSO4 + 2NaOH = CuSO4 + Cu(OH)2��(��������) �� ��
������ A D
����2. �������Ρ����Կ����Ƶ��������Ӷ����θ�Ѫѹ�ȼ������Ʊ��������Ρ���ʳ������NaCl�а����䷽��������ʳ��KCl������ijЩ��������Ϊ�ı䡰�����Ρ���ζ�����������þ��(����MgSO4��MgCl2).
����(1)���ij�������Ρ���Ʒa�к���NaCl��KCl������������Ϊ50%������Ʒa��ˮ��Һ�У��������������ǡ�������(�����ӷ���)��
����(2)̽��ij�������Ρ���Ʒb���Ƿ�����þ�Σ��Լ����ӵ��Ǻ���þ��(MgSO4��MgCl2�е�һ��)�������ʵ�鷽����������б���
������ѡ�Լ���BaCl2��Һ��NaOH��Һ��AgNO3��Һ������ˮ














 �����ǽ��ἰʱ������
�����ǽ��ἰʱ������