1、右图为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3个,下说法中不正确的是(A )

A.原子半径大小顺序是c>b>d>a
B.d的氢化物比a的氢化物稳定
C.a和d的原子结合可以形成带3个负电荷的阴离子
D.a、b、c最高价氧化物对应水化物的酸性强弱关系是c>b>a
2、下列关于ⅠA族和ⅡA族元素的说法正确的是( B )
A.ⅠA族和ⅡA族的元素均为金属元素
B.在同一周期中,单质和水反应,ⅠA族比ⅡA族剧烈
C.在同一周期中,单质的熔点,ⅠA族比ⅡA族高
D.ⅠA族和ⅡA族阳离子核外电子排布和同周期的稀有气体原子相同
3、16.几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是( A )
A.T的氢化物沸点高于Q的氢化物沸点 B.L、M的单质和稀盐酸反应速率:M > L
C.T、Q的氢化物常态下均为无色气体 D.L、Q形成的简单离子核外电子数相等
4.X、Y均为短周期元素,且X为ⅠA族元素,Y为ⅥA族元素。下列说法正确的是( C )
A.X的原子半径大于Y的原子半径
B.由X、Y组成的离子化合物中阴离子核外有18个电子
C.X2Y可能是离子化合物,也可能是共价化合物
D.由X、Y组成的化合物,溶于水后溶液呈碱性
5(08东城一模-10)、使用元素周期律分析下列推断,其中正确的组合是( B )
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)和铝同主族,其单质既能和盐酸反应,又能和氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A、①③④ B、①③⑥ C、③④⑤ D、②④⑥
6、右图是元素周期表的一部分,下列说法中正确的是( D )
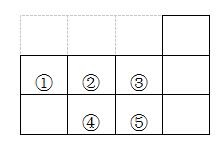
A.元素①位于第二周期第ⅣA族
B.气态氢化物的稳定性:④>②
C.元素的最高正化合价:③=⑤
D.最高价氧化物对应水化物酸性:⑤>④
7、已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( B )
A.质子数:c>b B.氢化物的稳定性:H2Y
C.离子的还原性:Y2-
8、(09年北京丰台)下列有关比较,大小顺序排列错误的是( B )
①热稳定性:PH3>H2S> HBr>NH3
②碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3
③物质的熔点:石英>食盐>汞>硫
④结合质子(H+)的能力:OH-> CO 32->CH3COO->SO42-
A.①②B. ①③ C. ②④ D.③④
9、已知X、Y、Z、W四种短周期元素(均非稀有气体元素)在周期表中的相对位置如下图所示,下列说法正确的是( B )
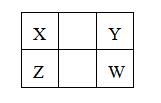
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
10、下列说法中正确的是( D )
A.同一周期元素的原子,半径越小越容易失去电子
B.在同一周期中,ⅠA族单质的熔点比ⅡA族的高
C.所有主族元素的最高化合价数和它的族序数数值相等
D.同主族元素的气态氢化物,相对分子质量越大,沸点不一定越高