
1、“骨质疏松症”是由人体缺钙引起的,可服用补钙剂来治疗。乳酸钙(CaC6H10O6・5H2O)是一种常见的补钙剂,出售乳酸钙片剂每片含乳酸钙200mg.一个成年缺钙病人每天服用20片乳酸钙片剂可达到补钙目的。计算:(计算结果保留整数)
(1) 乳酸钙中各元素的质量比。
(2) 该成年缺钙病人改用喝牛奶(每100mg牛奶中含钙0.104g)来补钙,每天至少需喝多少毫升牛奶。
2、生铁和钢都是铁合金,生铁中碳的含量在2.0%~4.3%之间,钢中碳的含量在0.03%~2%之间。将一块质量为10.0g的铁合金放入锥形瓶中,再向锥形瓶中加入100g稀H2SO4,恰好使铁合金中的铁完全反应(碳不熔于稀硫酸;铁合金中其他元素含量很低,可忽略不计),测得生成H2的体积为4.00L(H2在该条件下的密度为0.0880g/L)。试根据计算回答:(计算结果保留三位效数字)
(1)该铁合金是生铁还是钢?
(2)反应后所得溶液的溶质质量分数。
3、将3.1克氧化钠加到质量为m的水中,完全反应后,得到溶质的质量分数为16%的溶液,在该溶液中加入50克稀盐酸,两者恰好完全反应。(氧化钠与水反应的化学方程式为:Na2O+H2O==2NaOH)。求:
(1) m的值
(2) 所加盐酸中溶质的质量分数。
(3) 若要使反应后的氧化钠溶液成为20ºC时的饱和溶液,至少要蒸发掉多少克水?(20ºC时,氧化钠的溶解度为36克)
4、以下是我省生产的某种加钙食盐包装标签上的部分文字。请仔细阅读后回答以下问题:
|
配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:500g 成份表:氯化钠≥88% 钙(以Ca计)(0.5 ~ 1.3)% 碘(以I计)(20 ~ 50)mg/kg |
(1) 包装标签上钙含量是指___________(填单质钙、碳酸钙、钙元素中的一种)
(2) 为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是___________.
(3) 为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳。请计算此加钙食盐中钙元素的质量分数.
5、向盛有12.60g碳酸氢钠固体的烧杯中,加入100.5g硫酸溶液恰好反应。反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示。烧杯连同药品的起始质量为200.0g。反应的化学方程式为:
2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑
回答下列问题:
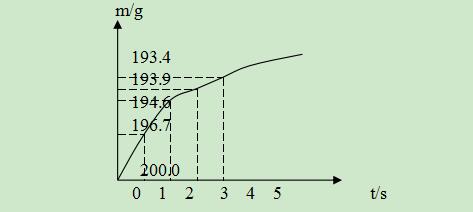
(1)当碳酸氢钠与硫酸溶液恰好完全反应时,所需的时间约为_________
(2) 当碳酸氢钠与硫酸溶液完全反应时,所产生二氧化碳的质量为_________。
(3) 反应后,所得硫酸钠溶液的溶质量分数为多少?
参考答案:
1、(5分)(1)解:m(Ca):m(C):m(H):m(O)=40×12×6:1×20:1611
=10:18:5:44
(2)解:设该缺钙病人每天至少需喝牛奶的体积为x
钙的质量分数为:(40/308)×100%=13%
(x×0.104g)/100mL=0.2g×20×13%
x=500nL
2、(6分)(1)解:设该铁合金中铁的质量为x
(H2)=4.00L×0.0880g/L=0.352g
Fe+H2SO4====FeSO4+H2↑
56 2
x 0.352g
x=(56×0.352g)/2=9.856g
该铁合金中碳的质量分数为(10.0g-9.856g)/10.0g×100%=1.44%
介于0.03%~2.0%之间,该铁合金是钢
(2)解:设反应后所得溶液中的质量为y
Fe+H2SO4 ==FeSO4+H2↑
152 2
y 0.352g
y=(152×0.352g)/2=26.75g
FeSO4的质量分数为:
26.75g/(100g+9.856g-0.352g)×100%=24.4%
3、(6分)解:(1)根据题意,设生成NaOH的质量为x
Na2O+H2O==2NaOH
62 80
3.1g x
62:80=3.1g:x x=4g
4g/(3.1g+m)=16% m=21.9g
(2)设盐酸中溶质的质量分数为y,生成NaCl的质量为a
HCl + NaOH ===NaCl
36.5 40 58.5
50g・y 4.0g a
36.5:40=50g・y:4.0g y=7.3%
(3)40:58.5=4.0g:a a=5.85g
设蒸发质量为b的水后可得到20˚C时NaCl的饱和溶
5.85g/(50g+25g-5.85g-b)=36/100
b=52.9g
答:(1)m为21.9g。(2)盐酸中溶质的质量分数为7.3%
(3)需蒸发52.9g水
4、(5分)(1)钙元素; (2)醋(或水);
(3)解:设产生0.132g二氧化碳所需CaCO3的质量为x
CaCO3 +2HCl===CaCl2 + H2O + CO2↑
100 44g
x 0.132g
100/x=44/0.132g x=0.3g
Ca元素质量:0.3g×(40/100)=0.12g
Ca元素质量分数:(0.12g/10g)×100%=1.2%
答:此加钙食盐中钙元素的质量分数为1.2%
5.(8分)(1)4s (2)6.6g
(3)设完全反应时,生成硫酸钠的质量为x
2NaHCO3 + H2SO4 ====Na2SO4 + 2H2O+ 2CO2↑
142 88
x 6.6g
142/88=x/6.6g x=10.65g
m(Na2SO4溶液)=12.60g+100.5g-6.6g=106.5g
w(Na2SO4)=(10.65g/106.5g)×100%=10%
答:所得硫酸钠溶液的溶质质量分数为10%
 ,我们将会及时处理。
,我们将会及时处理。