����1.����������Ȼ��ƺ�̼�����ڲ�ͬ�¶�ʱ���ܽ�ȣ����ݴ˱��ƶϺ�������(����)
|
�¶�/�� |
10 |
20 |
30 |
40 |
|
�ܽ��/g |
�Ȼ��� |
35.8 |
36.0 |
36.3 |
36.6 |
|
̼���� |
12.2 |
21.8 |
39.7 |
49.6 |
����A.20��ʱ����100gˮ����30g̼�����У���ֽ����õ���������Һ
����B.20��ʱ����100gˮ����30g�Ȼ����У���ֽ����������Һ��������������Ϊ30%
����C.�����ʵ��ܽ��������20�橁30��֮��Ӧ���ֽ���
����D.���Բ��ý��½ᾧ�ķ����Ӷ��ߵĻ�������ᴿ�Ȼ���
��������𡿽⣺A��20��ʱ��̼���Ƶ��ܽ��Ϊ21.8g����100gˮ����30g̼�����н����в���̼���Ʋ����ܽ⣬�õ����DZ�����Һ���ʴ���;
����B��20��ʱ���Ȼ��Ƶ��ܽ��Ϊ36g����100gˮ����30g�Ȼ����У���ֽ����������Һ��������������Ϊ��30g/(100g+30g)��100%=23.1%���ʴ���;
����C�����������ʵ��ܽ�����߱仯���ƿ��Կ�����20�橁30��֮��������Ӧ���ֽ��㣬����ȷ;
����D��̼���Ƶ��ܽ�����¶ȵ�Ӱ��仯���Ȼ��Ƶ��ܽ�����¶�Ӱ�첻������̼������Һ�л����������Ȼ��ƣ���ͨ�����½ᾧ(����ȴ�ȵı�����Һ)�ķ����ᴿ;���Ȼ�����Һ�л���������̼���ƣ���ͨ�������ᾧ�ķ����ᴿ���ʴ���;
������ѡC.
����2.10��ʱ��50gˮ������ܽ������10g��20��ʱ100gˮ������ܽ�������20g����ס��������ʵ��ܽ��Ϊ(����)
����A.��>�� B.��=�� C.��<�� D.���Ƚ�
��������𡿽⣺�ܽ�ȵĴ�С���¶��йأ���Ϊ�������������������¶Ȳ�ͬ�������ܽ�������Ƚϵģ�
������ѡD
����3.�ڲ�ͬ�¶��£���һ������NaCl��KNO3�ֱ����100gˮ�У�ʵ�������¼���±��У��йؽ�����ȷ����(����)
|
��� |
�¶� |
�ܽ���� |
|
ʵ��1 |
20�� |
����ܽ�36g NaCl |
����ܽ�31.6g KNO3 |
|
ʵ��2 |
40�� |
����36g NaClȫ���ܽ� |
����31.6g KNO3ȫ���ܽ� |
|
ʵ��3 |
80�� |
����ܽ�38.4g NaCl |
����ܽ�169g KNO3 |
����A.KNO3���ܽ�����һ������NaCl
����B.40��ʱNaCl���ܽ��һ������KNO3���ܽ��
����C.��ʵ��3������Һ�ֱ�����20�������Һ�����ʵ�������NaCl
����D.��ʵ��2������Һ�ֱ�������80�����Һ��Ũ�ȣ�NaCl>KNO3
��������𡿽⣺A����ʵ�������¼����֪��20�棬100gˮ������ܽ�36gNaCl��������ܽ�31.6gKNO3����20�棬KNO3���ܽ�����һ��С����NaCl����ѡ��˵������.
����B��40�棬100gˮ�м���36gNaClȫ���ܽ⣬����31.6gKNO3Ҳȫ���ܽ⣬�����ڲ�֪��Һ�Ƿͣ����Ƚ�NaCl��KNO3���ܽ�ȴ�С����ѡ��˵������.
����C��20�棬100gˮ������ܽ�36gNaCl��������ܽ�31.6gKNO3����20�棬�Ȼ��Ƶ��ܽ�ȴ�������ص��ܽ�ȣ���ʵ��3������Һ�ֱ�����20�������Һ�����ʵ�����NaCl>KNO3����ѡ��˵������.
����D��80��100gˮ������ܽ�38.4gNaCl������ܽ�169gKNO3;ʵ��2������Һ��40��100gˮ�м���36gNaClȫ���ܽ⡢����31.6gKNO3ȫ���ܽ��γɵ���Һ����ʵ��2������Һ�ֱ�������80���������Һ�����δ�����ı䣬����Һ��Ũ��NaCl>KNO3����ѡ��˵����ȷ.
������ѡD.
����4.��֪������������ݶ�����20��ʱ����.
������ȡ110g NH4Cl������Һ������10gˮ����������3.72g;
�����ڽ�120g NaNO3������Һ��50g NaNO3���干����һ���ձ��У��ټ���50gˮ����Һ��Ȼ���ͣ���ʣ��6g����û���ܽ�;
������NaCl������Һ����������Һ��������Ϊ36��136.
������20��ʱ3�����ʵ��ܽ���ɴ�С��˳��Ϊ(����)
����A.�٢ڢ� B.�ڢ٢� C.�ۢ٢� D.�٢ۢ�
��������𡿽⣺�ٴӡ�ȡ110g 20��ʱ��NH4Cl������Һ������10gˮ����������3.72g����֪�����¶�ʱ100gˮ����ܽ�37.2gNH4Cl;
�����ڴ���˵����20��ʱ(50g��6g)NaNO3�����ܽ���50gˮ����Һǡ�ñ���;����20��100gˮ������ܽ�88gNaNO3����;
��������20��ʱNaCl������Һ����������Һ��������Ϊ36��136��������20��ʱNaCl������Һ���������ܼ���������Ϊ36��100.���20��ʱ3�����ʵ��ܽ���ɴ�С��˳��Ϊ���ڢ٢�.
������ѡB.
����5.��20��ı��ͳ���ʯ��ˮ��Ͷ�������������Ʒ�ĩ����ַ�Ӧ������˵���������(����)
����A.��Һ�¶�δ��ȴ��20��ʱ��һ���DZ�����Һ
����B.��Һ�¶�δ��ȴ��20��ʱ����������������ԭ��Һ��
����C.��Һ�¶Ȼָ���20��ʱ����Һ������ԭ��ҺС
����D.��Һ�¶Ȼָ���20��ʱ����������������ԭ��Һ�����
��������𡿽⣺A���������Ƶ��ܽ�����¶ȵ����߶���С����������ˮ��Ӧ���ȣ�ʹ�¶����ߣ��������Ƶ��ܽ�ȼ�С����A��ȷ;
����B����Һ�¶�ĩ��ȴ��20��ʱ���������Ƶ��ܽ��С��20����ܽ�ȣ����������������ȼ���ҺС����B����;
����C������������ˮ��Ӧ�����������ƣ������˱�����Һ�е��ܼ���ʹ������������������������Һ������С����C��ȷ;
����D����Һ�¶Ȼָ���20��ʱ����Ϊ�������Ƶı�����Һ��ͬ����ͬ��������ͬ���ܼ��еı�����Һ��������������ͬ����D��ȷ��
������ѡ��B.
����6.��ͼ�Ǽס������ֹ������ʵ��ܽ������.����˵������ȷ����(����)
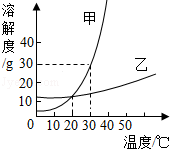
����A.���ܽ�ȴ����ҵ��ܽ��
����B.30��ʱ���ı�����Һ�����ʵ���������Ϊ30%
����C.�����ʵ��ܽ�����¶ȱ仯��Ӱ���С�������ʵ��ܽ�����¶ȱ仯��Ӱ��ϴ�
����D.���к���������ʱ���������ܼ��ķ����ᴿ��
��������𡿽⣺A���Ƚ��ܽ��Ӧ˵���¶ȣ���˵���¶ȱȽ������壬�ʴ�ѡ�����.
����B�����¶������ʵ��ܽ��30g�����Ը��¶������ʵ���������=30/130��100%=23%���ʴ�ѡ�����.
����C���ܽ�����¶ȱ仯�����֪���������������ԣ����Ҳ����ԣ��ʴ�ѡ����ȷ.
����D�����ڼ��ܽ�����¶ȵ����߶����������ҵ��ܽ�����¶ȵ�Ӱ���С����˿���ͨ�����½ᾧ�ķ������ᴿ�����ҵļף��ʴ�ѡ�����.
������ѡC
����7.a��b�������ʵ��ܽ��������ͼ��ʾ������˵������ȷ����(����)
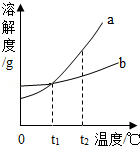
����A.Ҫʹ�ӽ����͵�b��Һת��Ϊ������Һ���ɲ���������Һ�ķ���
����B.t2��ʱ���������ʵı�����Һ��������������a>b
����C.��t2��ʱa�ı�����Һ������t1�棬��Һ��������
����D.��t2��ʱa��b�ı�����Һ�ֱ�����t1�棬����Һ�����������������
��������𡿽⣺A��ͨ�������ܽ�����߿�֪��Ҫʹ�ӽ����͵�b��Һת��Ϊ������Һ���ɲ��������ܼ��ķ�������A��ȷ;
����B��t2��ʱ��a���ʵ��ܽ�ȴ���b���ʵ��ܽ�ȣ������������ʵı�����Һ��������������a>b����B��ȷ;
����C�������¶ȣ�a���ʵ��ܽ�ȼ�С�����Խ�t2��ʱa�ı�����Һ������t1�棬��Һ������С����C����;
����D��t1��ʱ��a��b���ʵ��ܽ����ȣ����Խ�t2��ʱa��b�ı�����Һ�ֱ�����t1�棬����Һ����������������ȣ���D��ȷ.
������ѡ��C.
����8.ͼ��A��B��C���ֹ������ʵ��ܽ������.����˵����ȷ����(����)
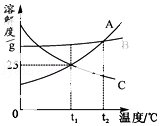
����A.t1��ʱ��A�ı�����Һ��������������Ϊ25%
����B.t2��ʱ��A��B��C�������ʵı�����Һ���µ�t1��������Һ���������������Ĺ�ϵΪB>C=A
����C.��t1��ʱA��C�ı�����Һ���µ�t2��ʱ��A��C����Һ�����ɲ�������Һ
����D.��t2��ʱA��B��C�������ı�����Һ���µ�t1��ʱ�������������������A
��������𡿽⣺A��t1��ʱ��A���ʵ��ܽ����25g������A�ı�����Һ��������������Ϊ��25/(100+25)��100%=20%����A����;
����B��t1��ʱ��B���ʵ��ܽ�����A���ʵ��ܽ�ȴ�֮�������¶ȣ�A��B���������壬C���ʲ����������壬����t2��ʱ��A��B��C�������ʵı�����Һ���µ�t1��������Һ���������������Ĺ�ϵΪB>A>C����B����;
����C���Թ��¶ȣ�C���ʵ��ܽ�ȼ�С�����Խ�t1��ʱA��C�ı�����Һ���µ�t2��ʱ��C���ʶ����ɲ�������Һ����C����;
����D��A���ʵ��ܽ�����¶ȱ仯Ӱ��ϴ����Խ�t2��ʱA��B��C�������ı�����Һ���µ�t1��ʱ�������������������A����D��ȷ.
������ѡ��D.
����9.ͼ�Ǽס��ҡ������ֹ������ʵ��ܽ������.���������������(����)
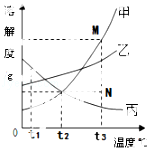
����A.t2��ʱ���������ʵ��ܽ�ȴ�С˳��Ϊ����>��=��
����B.t2��ʱ���ס����������ʵ���Һ�����ʵ������������
����C.���������л��������������ʣ����ý��½ᾧ�ķ����ᴿ��
����D.���ý����¶ȵķ������ɽ����͵ı�������Һ��ɲ�����
��������𡿽⣺A�����ܽ�����߿�֪��t2��ʱ���������ʵ��ܽ�ȴ�С˳��Ϊ����>��=����ȷ����ȷ�����������⣬��ѡ�����;
����B��t2��ʱ���ס����������ʵ���Һ�����ʵ�����������ȴ�����Ϊû��ָ���DZ�����Һ������������⣬��ѡ����ȷ;
����C�����������л��������������ʣ����ý��½ᾧ�ķ����ᴿ�ף���Ϊ�����¶ȵ�Ӱ��仯�Ƚϴ���ȷ�����������⣬��ѡ�����;
����D�����ý����¶ȵķ������ɽ����͵ı�������Һ��ɲ����ͣ���Ϊ�����ܽ�����¶ȵ����߶����٣���ȷ�����������⣬��ѡ�����;
������ѡB
����10.��ͼ��ʾ�ס��ҡ����������ʵ��ܽ�����ߣ�����˵����ȷ����(����)
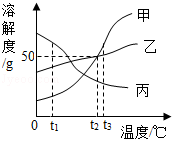
����A.t2��ʱ���ס�����Һ��������������һ�����
����B.���к��������ף��ɲ��ý��½ᾧ�ķ����ᴿ��
����C.t3��ʱ���ס��ҡ����������ʵı�����Һ���µ�t1�棬������Һ���������������Ĵ�С��ϵΪ��>��>��
����D.t2��ʱ��100g�ı�����Һ�м���400gˮ���õ�10%�ļ���Һ
��������𡿽⣺A����֪��Һ�����ʡ��ܼ����������٣����ж����ʵ����������Ƿ����;�ݱ���ʱ���������ļ���ʽ���ܽ��/(100g+�ܽ��)��100%��֪��������Һ�DZ�����Һ�����¶��¶��ߵ��ܽ����ȣ������ʵ������������;�ʴ���;
����B���ҵ��ܽ�����¶ȵı仯�������к��������ף��ɲ��������ᾧ�ķ����ᴿ�ң��ʴ���;
����C����t3��ʱ�������ļס��ҡ����������ʵı�����Һͬʱ���µ�t1�棬�������������������䣬���ҵĶ��о������������������������С������ͼ����Կ�������t1��ʱ�ס��ҡ����������ʵ��ܽ������>��>�ף��������ʵı�����Һ���������������Ĵ�С��ϵ����>��>�ף�����ȷ;
����D��t2��ʱ��100g�ı�����Һ���������ʵ�����=50*100/150��33g������400gˮ��������Һ��������������=33/(100+400)��100%��6.7%�����õ�10%�ļ���Һ���ʴ���.
�����𰸣�C
����11.��ͼ�Ǽס��ҡ����������ʵ��ܽ�����ߣ�����˵������ȷ���ǡ���)
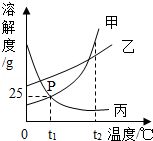
����A.P���ʾ�ס����������ʵı�����Һ�������
����B.t1��ʱ�������ʵı�����Һ��������t2��ʱ���DZ�����Һ
����C.t1��ʱ�������ʵı�����Һ�����ʺ��ܼ���������Ϊ1��4
����D.���������ʵ���Һ��t2�潵��t1�棬�������������Ǽ�����
��������𡿽⣺A��P���ʾ�ס����������ʵı�����Һ����������������ȣ���A����;
����B�������ʵ��ܽ�����¶ȵ����߶���������t1��ʱ�������ʵı�����Һ��������t2��ʱ���ɲ�������Һ����B����;
����C��t1��ʱ�������ʵ��ܽ����25g�����Լ����ʵı�����Һ�����ʺ��ܼ���������Ϊ25g��100g=1��4����C��ȷ;
����D�����������ʵ���Һ��������ȷ�������Դ�t2�潵��t1�棬��������Ķ��ٲ���ȷ������D����.
������ѡ��C.
����12.��ͼ�Ǽס��ҵ��ܽ�����ߣ�����˵������ȷ����(����)
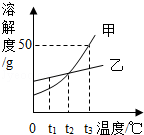
����A.t1��ʱ���ҵ��ܽ�ȴ��ڼ��ܽ��
����B.t2��ʱ���ס��ұ�����Һ�����������������
����C.�����¶���ʹ�ӽ����͵ļ���Һ��Ϊ������Һ
����D.t3��ʱ��75g�ı�����Һ�м���50gˮ�����Եõ���������Ϊ25%����Һ
��������𡿽⣺A����ͼ��֪��t1��ʱ���ҵ��ܽ�ȴ��ڼ��ܽ�ȣ���ȷ;
����B��t2��ʱ���ס��ҵ��ܽ�����߽���һ�㣬�ܽ����ȣ�����Һ����������������ȣ���ȷ;
����C�����ܽ�����¶Ƚ��Ͷ���С�����Խ��¿�ʹ�䲻������Һ��Ϊ������Һ����ȷ;
����D��t3��ʱ���ܽ����50g����100gˮ������ܽ�50g�ף��γɱ�����Һ150g����75g�ı�����Һ����25g�ף���50gˮ�õ���Һ����������=25/125��100%=20%������25%���ʴ���;
������ѡ��D.
����13.��ͼ�Ǽס��ҡ����������ʵ��ܽ�����ߣ�����˵������ȷ����(����)
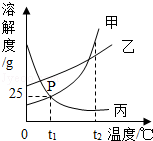
����A.t1��ʱ�������ʵı�����Һ�����ʺ��ܼ���������Ϊ1��4
����B.P���ʾ�ס����������ʵı�����Һ�������
����C.t1��ʱ�������ʵı�����Һ��������t2��ʱ���DZ�����Һ
����D.���������ʵ���Һ��t2�潵��t1�棬�������������Ǽ�����
��������𡿽⣺A��t1��ʱ�������ʵ��ܽ����25g�����Լ����ʵı�����Һ�����ʺ��ܼ���������Ϊ25g��100g=1��4����A��ȷ;
����B��P���ʾ�ס����������ʵı�����Һ����������������ȣ���B����;
����C�������ʵ��ܽ�����¶ȵ����߶���������t1��ʱ�������ʵı�����Һ��������t2��ʱ���DZ�����Һ����C����;
����D���������ʱ�����Һ����������ȷ�������Խ��������ʵ���Һ��t2�潵��t1�棬�����������������ȷ������D����.
������ѡ��A.
����14.��ͼΪ�ס��������ʵ��ܽ�����ߣ�����˵����ȷ����(����)

����A.�ס��������ʾ�������������
����B.�����ʵ��ܽ�ȴ��������ʵ��ܽ��
����C.t1��ʱ���ס��������ʱ�����Һ�����������������
����D.t2��ʱ�������ʱ�����Һ��������������Ϊ50%
��������𡿽⣺A��ͨ�������ܽ�����߿�֪����10��ʱ���ס������ʵ��ܽ�ȴ���10g�����Լס��������ʾ������������ʣ���A����;
����B���ڱȽ����ʵ��ܽ��ʱ����Ҫָ���¶ȣ���B����;
����C��t1��ʱ���ס��������ʵ��ܽ����ȣ����Ա�����Һ����������������ȣ���C��ȷ;
����D��t2��ʱ�������ʵ��ܽ����50g�����Լ����ʱ�����Һ��������������Ϊ50/150��100%=33.3%����D����.
������ѡ��C.
����15.����ˮƿ�ǣ��д����������ĭ�ݳ�������˵������ȷ����(����)
����A.���ʼ��� B.�ܽ�ȼ�С
����C.Ũ�ȼ�С D.������Һ��ɲ�������Һ
��������𡿽⣺������ܽ������ѹǿ���������������ѹǿ�ļ�С����С.����ˮƿ��ʱ��ѹǿ��С��ԭ���ܽ�Ķ�����̼������ܽ�ȼ�С��һ���ֶ�����̼�ݳ�����Һ�����ʡ�Ũ�ȼ�С���ݳ���Ķ�����̼��Һ��Ȼ�DZ�����Һ.���ԣ�A��B��C��ȷ��D����.
������ѡD.




















 �����ǽ��ἰʱ������
�����ǽ��ἰʱ������