2016��ʦ�ʸ��Ը��С���ѧѧ�ơ��ر�֪ʶ��һ��
����1�������ᡢ��ָʾ���ı�ɫ��Χ��
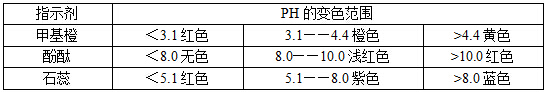
����2���ڶ��Ե缫�ϣ��������ӵķŵ�˳��
��������(����ӵ�����)��Au3+ >Ag+>Hg2+ >Cu2+ >Pb2+ >Fa2+ >Zn2+ >H+ >Al3+>Mg2+ >Na+ >Ca2+ >K+
��������(ʧ���ӵ�����)��S2- >I- >Br�C >Cl- >OH- >�������
����ע�⣺���ý��������������ʱ������������������ԭ��Ӧ(Pt��Au����)
����3��˫ˮ�����ӷ���ʽ����д��
����(1)���д��ˮ������ӣ��ұ�д��ˮ�����;
����(2)��ƽ�����������ƽ��ɣ������ұ���ƽ����ԭ��;
����(3)H��O��ƽ�����DZ�ˮ��
����������Na2CO3��AlCl3��Һ���ʱ�� 3 CO32- + 2Al3+ + 3H2O = 2Al(OH)3�� + 3CO2��
����4��д����ܷ�Ӧ����ʽ�ķ�����
����(1)��������Ӧ���������ʲô;(2)��ƽ��
�����������KCl��Һ��2KCl + 2H2O == H2��+ Cl2��+ 2KOH
����5����һ����ѧ��Ӧ����ʽ��д�ɶ����缫��Ӧ�ķ�����
����(1)�����ӵ�ʧд�������뷴Ӧʽ;(2)�ٿ��Ƿ�Ӧʱ�Ļ���(���Ի����);(3)ʹ���ߵ�ԭ�������������ȡ�
��������д����Ϊԭ���(�ŵ�)ʱ�ĵ缫��Ӧ��
����д�������뷴Ӧ�� Pb �C2e- �� PbSO4 PbO2 +2e- �� PbSO4
���������������Ի����У���������ԭ�ӣ�ӦΪ��
����������Pb + SO42- -2e- = PbSO4
���������� PbO2 + 4H+ + SO42- +2e- = PbSO4 + 2H2O
����ע�⣺���dz��ʱ���ǵ�⣬�缫��Ӧ��Ϊ���ϵ缫��Ӧ�ĵ�ת��
������ ������PbSO4 +2e- = Pb + SO42- ������PbSO4 + 2H2O -2e- = PbO2 + 4H+ + SO42-
����6���ڽ�������г��õ��ĺ�ȣ�ԭ�Ӻ�ȡ����Ӻ�ȡ����Ӻ�ȡ���ɺ�ȡ�������ȡ��õ��ķ����У������غ㡢����������һ������������ϵ����ʮ�ֽ��� ���㷨��(��������ԭ��Ӧ��ԭ���غ㡢��� ƽ�⡢����ƽ���õö࣬������ԭ��Ӧ�������غ��õö�)
����7�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�࣬���Ӱ뾶ԽС��
����8��������۵㣺ԭ�Ӿ��� >���Ӿ��� >���Ӿ���
������ѧѧ����ԭ�Ӿ����У� Si��SiC ��SiO2�ͽ��ʯ��
����ԭ�Ӿ�����۵�ıȽ�����ԭ�Ӱ뾶Ϊ���ݵģ� ���ʯ > SiC > Si (��Ϊԭ�Ӱ뾶��Si> C> O)��
����9�����Ӿ�����ۡ��е㣺��ɺͽṹ���Ƶ����ʣ�������Խ���ۡ��е�Խ�ߡ�
����10������Ĵ��磺һ��˵�������������������������Ľ������Ӵ����磬�ǽ����������������Ľ������Ӵ����硣
����11������Fe3+����Һһ������ԡ�
����12�����γ���������ʣ�H2O ��NH3 ��HF��CH3CH2OH ��
����13����ˮ(�Ҵ���Һһ��)���ܶ�С��1��Ũ��Խ���ܶ�ԽС��������ܶȴ���1��Ũ��Խ���ܶ�Խ��98%��Ũ������ܶ�Ϊ��1.84g/cm3��
����14�������Ƿ棺(1)�Ƿ��г������ɡ�����ų�;(2)�Ƿ��������������;(3)�Ƿ���������ԭ��Ӧ;(4)�Ƿ�����������[Fe(SCN)2��Fe(SCN)3��Ag(NH3)+��[Cu(NH3)4]2+ ��];(5)�Ƿ���˫ˮ�⡣
����15�������ܽ�ȣ���һ����ѹǿ���¶��£�1���ˮ��ﵽ����״̬ʱ����������
������ϵ�绰��4000-525-585 �γ���ѯ�źţ�W712931601��������ϵͨ��
�����ȵ��Ƽ�����ʦ�ʸ�֤����ʱ�估������� ��ʦ�ʸ�֤�������� ��Сѧ��ʦ�ʸ�֤����������ʦ�ʸ�֤�������� �й���ʦ�ʸ���
������Сѧ����ʦ�ʸ��Դ��(����) 2016��Сѧ��ʦ�ʸ��Ժϸ�֤�鲹�� 2016����Сѧ��ʦ�ʸ�֤���ѯ���
����С���Ƽ�����ʦ�ʸ�֤����ʱ�� ��ʦ�ʸ�֤���Կ�Ŀ���������� ��ʦ�ʸ�֤��������
������Դ������ʦ�ʸ�������רҵ�ʸ���������ʦ���ο�����Ṥ����˾������ְ�Ƽ����Ӫ��ʦ������ѯʦ��Ӥʦ��ҵ��λ��ʦ��Ƹ����Ա��ѡ�����о�����ѡ�������
�������ְ���м����ְ������ʦע����ʦ֤ȯ��ҵ���д�ҵ���ʵ��ͳ��ʦ���ʦ�����ʦ�����ҵ�ʸ�˰��ʦ�ʲ�����ʦ��������ʦACCA/CAT�۸��֤ʦͳ���ʸ��ҵ
һ������ʦ��������ʦ��������ʦ��۹���ʦ����ְ����·����ʦ�����˴�Աע�Ὠ��ʦ�������ʦ��������ʦ��ѯ����ʦ���ز�����ʦ ����滮ʦ�ṹ����ʦ��������ʦ��ȫ����ʦ�豸����ʦ����Ӱ���������صǼǴ�����·���ʦ��·����ʦ��������ʦůͨ����ʦ����ˮ����ʦ��������ʦ
ִҵҩʦִҵҽʦ�����ʸ���������ְ����ʿ�ʸ�֤������ʦ���ܻ�ʦסԺҽʦ�ٴ�ִҵҽʦ�ٴ�����ҽʦ��ҽִҵҽʦ��ҽ����ҽʦ����ҽҽʦ����ҽ������ǻִҵҽʦ��ǻ����ҽʦ��������ҽʦ��������ҽʦʵ�������ڿ�����ҽʦ�������ҽʦ��ҽ�ڿ�������������ҽʦ������ҽʦ��ҩʿ/ʦ��ҩʿ/ʦ�ٴ����鼼ʦ�ٴ�ҽѧ������ҽ����